燃料電池とは
水を電気分解すると水素と酸素になることは良く知られています。
燃料電池はこれとは逆に水素と空気中の酸素を化学反応させ、直接電気を取り出す新しいタイプの発電装置です。
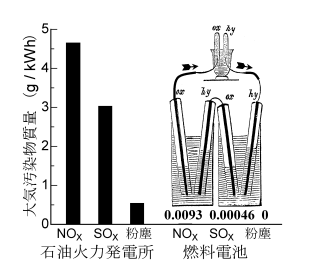
1839年、Grove卿によって燃料電池の最初の実験がなされました。右図のカットに示すように、希硫酸電解液の中に試験管を倒立させ、白金黒(白金微粒子)を付けた白金電極を差し込んだのです。まず、電気分解して、水素と酸素をためました。電解をやめた後、電圧計をつなぐと、水素がたまった電極が負極となって電圧が発生することを見つけました。そして、この燃料電池をいくつか直列に接続した電気エネルギーで、再び水が電気分解できることを確かめたのです。
燃料電池は、他の発電手段と異なりエネルギー変換の過程で熱エネルギーを経由しないため、高い効率を実現できます。
水素を燃料に用いれば環境汚染物質を全く排出しません。天然ガスなどを水素リッチなガスに改質して用いた場合でも、右図に示すように環境汚染物質の排出量を極めて低く抑えられます。
例えば、あなたが石油火力発電所からの電力を1 kWh使うと(コタツやホットプレートを1時間使い続ける)、4.6 gのNOxと3 gのSOxを大気中に放出したことになります(省エネルギーと環境汚染防止は一人一人の意識改革から!)。他方、燃料電池で発電すれば、NOxは約1/500に、SOxは約1万分の1に押さえ込めるのです。燃料を直接燃焼しないため、粉塵(ぜんそくや肺ガンのモト)の発生はゼロです。エネルギー変換効率が高いため、燃料の消費量が減って、地球温暖化作用が問題となっている炭酸ガスの排出量も約半分になります。

燃料電池は、一般電力用の発電所ばかりでなく、電気自動車(EV)の電源にも使えます。一定走行距離ごとに充電が必要な蓄電池式EVとは異なり、燃料を補給するだけで走り続けることができます。EVに燃料電池を用いた場合の総合エネルギー変換効率は、ガソリン車の約2.5倍です。下の表を見ても、燃料電池がいかにクリーンで省エネルギーに貢献するかわかっていただけると思います。
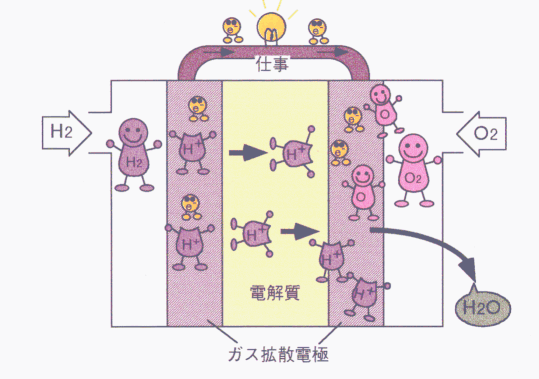
燃料電池は下図に模式的に示すように、電解質(液体または固体)と2つのガス拡散電極から構成されています。電極は、反応ガスをイオンと電子に分ける(またはその逆)機能を持ち、電解質は生じたイオンを通す役割を持ちます。
燃料電池は、電解質の種類によって、アルカリ型(AFC)、リン酸型(PAFC)、溶融炭酸塩型(MCFC)、固体酸化物型(SOFC)、そして、電気自動車用電源に最も期待されている高分子電解質型(PEFC)に分類されます。
私たちの研究室はこの分野で永年の研究実績を持ち、研究の範囲も燃料電池用新材料(電極触媒、電解質膜)の設計・合成から電池の性能・耐久性評価まで多岐にわたっています。これまでに発表した研究成果は国内外で高く評価され、国際的な研究交流も盛んです。
最近では、燃料電池に加えて、固体高分子形の水電解デバイスの研究にも力を入れています。


